【前沿资讯】基因编辑新动向——FGFR1、BRD4和BACE1基因敲除细胞

基因敲除细胞是指利用CRISPR技术进行基因编辑,通过设计特定的sgRNA靶向目标基因的剪切位点,使Cas9蛋白与sgRNA结合并将目的基因从细胞中“剪切”掉,从而实现基因敲除。基因敲除细胞在生命科学、医学和药物研发等领域都有着广泛的应用前景,如利用基因敲除技术建立疾病模型、进行药物筛选和靶点验证、敲除致病基因实现对疾病的基因治疗等。本文选取三篇基因敲除细胞的相关研究为大家进行解读,带您了解这一前沿技术的最新进展。
一、FGFR1基因敲除验证FGFR1-ERK1/2-AKT信号通路在乳腺癌细胞中的具体作用
原文链接:https://doi.org/10.3390/cells8030223
成纤维细胞生长因子(Fibroblast Growth Factor, FGF)—成纤维细胞生长因子受体(Fibroblast Growth Factor Receptor, FGFR)信号轴是介导肿瘤基质与癌细胞之间相互作用的主要信号传导途径之一,FGFR1的激活可以通过转位、点突变或FGFR1基因的扩增导致癌症恶化。此外,G蛋白偶联雌激素受体(GPER, GPR30)也被确认为介导雌激素在多种病理生理条件下作用的受体。
为探索GPER如何通过FGF2/FGFR1信号轴介导CAFs与乳腺癌细胞之间的通讯,研究人员使用了CRISPR/Cas9基因编辑技术来敲除MDA-MB-231乳腺癌细胞中的成纤维细胞生长因子受体1(FGFR1),正常对照组中来自雌激素刺激的癌症相关成纤维细胞(CAFs)的条件培养基(CM)能够诱导FGFR1野生型(WT)MDA-MB-231细胞中CTGF(结缔组织生长因子)的表达,并通过FGFR1-ERK1/2-AKT信号通路促进细胞的迁移和侵袭。而在FGFR1基因敲除的MDA-MB-231细胞中,这种诱导作用则显著降低或消失。FGFR1基因敲除细胞揭示了GPER在肿瘤微环境中调节FGF2表达的新角色,证实了FGFR1在乳腺癌中的基因扩增与患者的整体存活率密切相关,表明FGFR1可能作为乳腺癌治疗的一个靶点,阐明了CAFs与乳腺癌细胞之间的旁分泌激活作用,为开发新的治疗策略提供了理论基础。
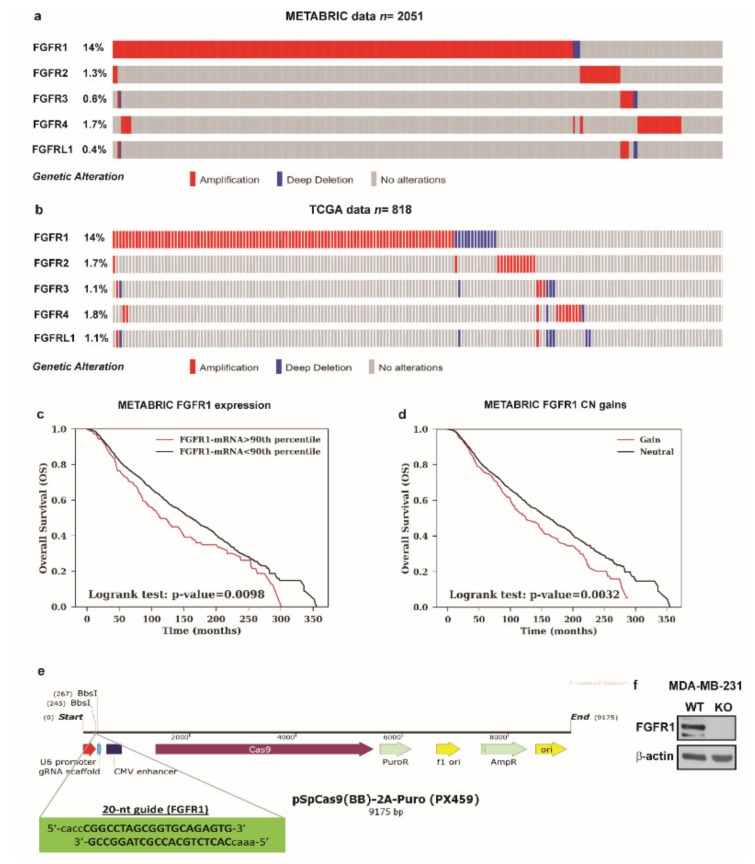
图1 MDA-MB-231细胞中METABRIC和TCGA数据集的分析和CRISPR/ cas9介导的FGFR1敲除
二、BRD4基因敲除细胞揭示皮肤鳞状细胞癌新的关键致癌蛋白
原文链接:https://doi.org/10.1016/j.cellsig.2017.10.010
近年来,皮肤鳞状细胞癌的发病率以惊人的速度上升,皮肤鳞状细胞癌和其它非黑色素瘤皮肤癌每年都会导致大量的人类死亡。统计研究表明,超过20%的世界人口在一生中可能会发展成皮肤癌,目前的治疗选择包括手术、放疗和/或化疗的组合,但对于晚期和/或转移性皮肤鳞状细胞癌的预后仍然不令人满意。最近的癌症研究提出BRD4可能是一个潜在的致癌蛋白,但其在皮肤鳞状细胞癌中的表达和生物学功能尚未被研究。
为了突破现有治疗方法的局限,研究人员开展了分子靶向治疗的研究,使用CRISPR/Cas9系统直接敲除BRD4基因。BRD4基因的敲除或沉默显著降低了皮肤鳞状细胞癌细胞(SCC)的增殖能力,导致SCC细胞中几个与细胞增殖密切相关的癌基因(如cyclin D1、Bcl-2和MYC)的表达显著下降。在体内实验中,通过CRISPR/Cas9介导的BRD4基因敲除显著抑制了A431细胞在严重联合免疫缺陷(SCID)小鼠中的肿瘤生长。BRD4基因敲除细胞为进一步的临床研究和药物开发提供了科学依据,有助于开发针对BRD4的分子靶向治疗药物。
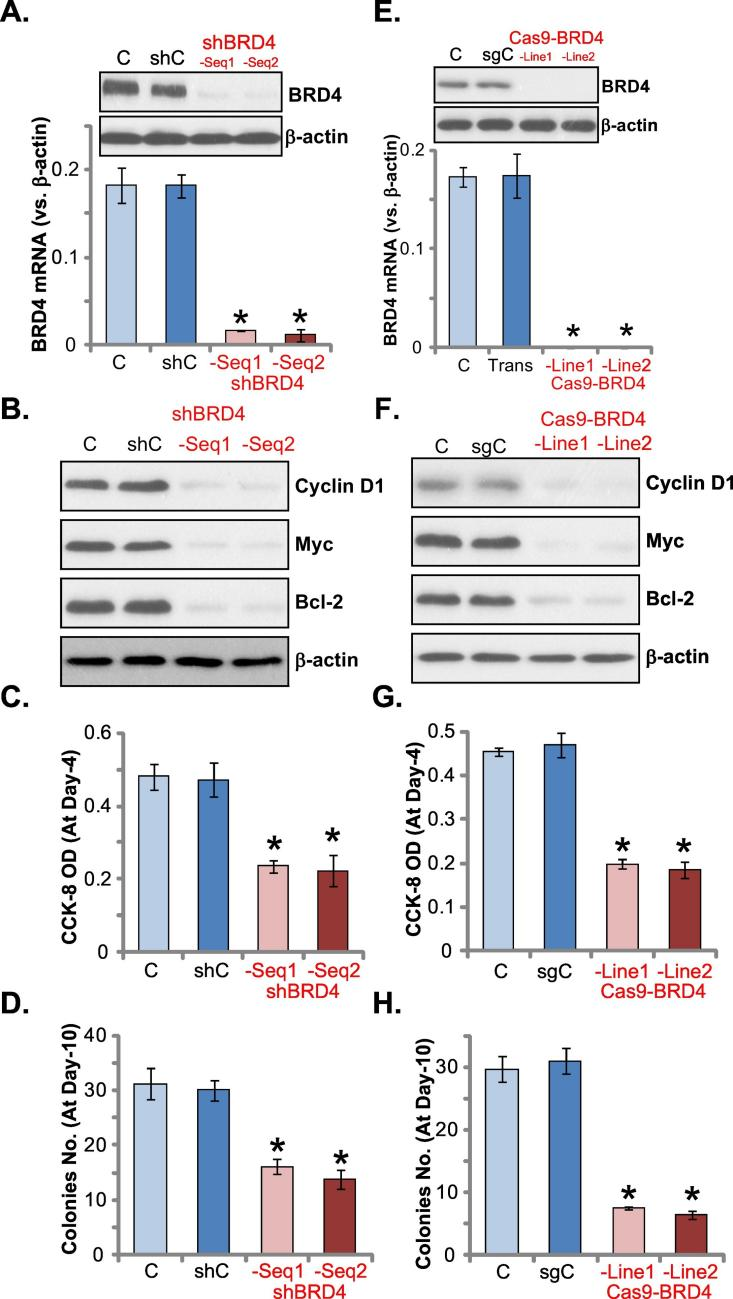
图2 BRD4沉默或敲除抑制A431细胞增殖
三、BACE1基因敲除细胞为阿尔茨海默病治疗提供新方法
原文链接:https://doi.org/10.1002/adma.202101993
阿尔茨海默病(Alzheimer's Disease, AD)是最常见的神经退行性疾病(Neurodegenerative Diseases, NDs),病理特征是淀粉样蛋白-β的异常聚集,这些聚集被认为是AD治疗的潜在靶点,但目前的治疗方法尚未能有效地清除淀粉样蛋白-β并阻止其再生。相关研究报道,抑制BACE1基因表达可以直接从源头抑制淀粉样蛋白-β再生,从而实现有效的AD治疗。
研究人员通过T7E1酶切实验,发现CF-TBIO(CRISPR/Cas9载体)在体外实验中对BACE1基因的敲除效率达到了41.1%,CF-TBIO处理的2xTg-AD(阿尔茨海默病转基因模型小鼠)显示出显著降低的BACE1蛋白表达,CF-TBIO和长期治疗组(LTIG)显著减少了淀粉样蛋白-β42的分泌,减少了淀粉样蛋白-β斑块的面积和数量。BACE1基因敲除细胞减少了淀粉样蛋白-β的产生,为AD的基因治疗提供了新的策略。
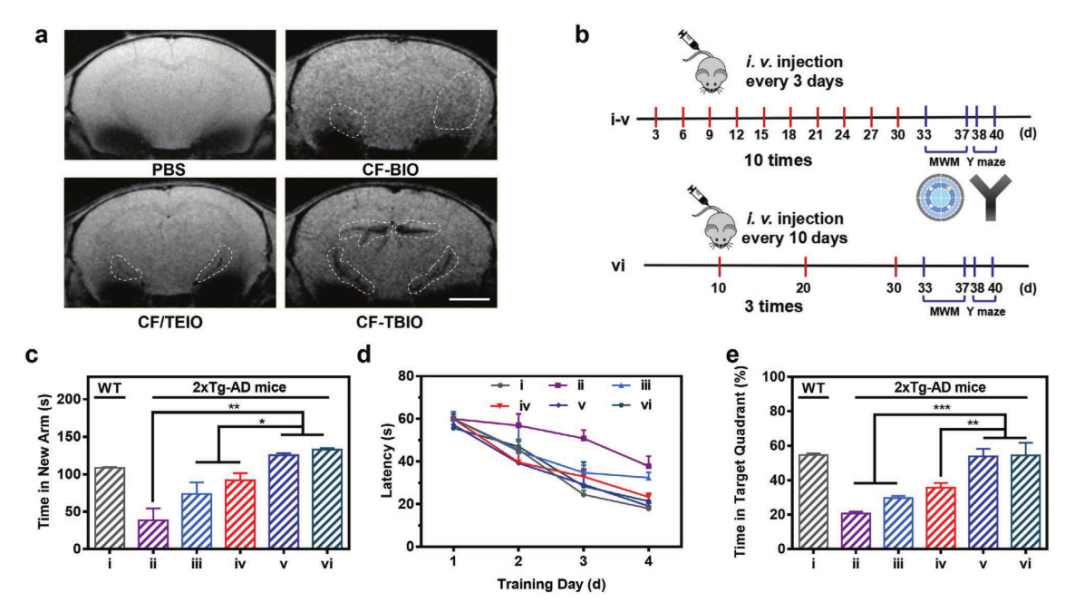
图3 xTg-AD小鼠BACE1、淀粉样蛋白-β表达水平及神经元修复能力的评价
艾迪基因拥有3800+基因敲除细胞现货,覆盖上述文章中的FGFR1、BRD4和BACE1等热门靶点细胞,为您提供一站式科研支持。现在下单,一周送达,4980元起!
没有现货,想自己做实验?艾迪基因实现技术突破,全新推出CRISPR Editx™KO敲除试剂盒,30min转染,48h观测编辑效率,千元实现敲除!
点击图片查看详情
近期资讯:
2.聊聊基因编辑技术的前世今生:ZFN、TALEN、CRISPR
联系我们
18102225074(微信同号)
market@edgene.cn




