【前沿资讯】基因编辑新动向——fut8、atm和brca1基因敲除细胞提供癌症治疗新视角

基因敲除细胞是指利用CRISPR技术进行基因编辑,通过设计特定的sgRNA靶向目标基因的剪切位点,使Cas9蛋白与sgRNA结合并将目的基因从细胞中“剪切”掉,从而实现基因敲除的细胞。基因敲除细胞在生命科学、医学和药物研发等领域都有着广泛的应用前景,如利用基因敲除技术建立疾病模型、进行药物筛选和靶点验证、敲除致病基因实现对疾病的基因治疗等。本文选取三篇基因敲除细胞的相关研究为大家进行解读,带您了解这一前沿技术的最新进展。
一、FUT8-KO细胞发掘胰腺癌治疗新靶点
原文链接:https://doi.org/10.1016/j.bbagen.2021.129870
胰腺导管腺癌(Pancreatic ductal adencarcinoma, PDAC)是一种极其恶性的肿瘤,占所有胰腺癌的90%。研究表明,癌细胞表面的异常糖基化变化与肿瘤进展和转移正相关,α1,6-岩藻糖基转移酶(FUT8)是负责催化核心岩藻糖基化的关键酶,其在多种恶性肿瘤中的表达和激活异常,与多种生理和病理过程相关,尽管FUT8在其他类型的癌症中的作用已被观察到,但其在PDAC恶性转化中的具体分子机制和作为潜在治疗靶点的可能性尚不清楚。
研究人员使用CRISPR/Cas9系统在MIA PaCa-2和PANC-1细胞中敲除FUT8基因,通过Transwell迁移实验和创伤愈合实验评估FUT8-KO细胞的迁移能力,通过MTT实验和集落形成实验评估FUT8-KO细胞的增殖能力,并检测了FUT8-KO细胞中癌症干细胞标志物的表达水平。结果显示,与野生型细胞相比,FUT8-KO细胞的迁移能力、增殖和集落形成能力显著降低,FUT8-KO细胞中癌症干细胞标志物的表达降低。FUT8基因敲除细胞揭示了FUT8在胰腺癌中的重要作用,证明了FUT8可能是胰腺癌治疗的一个潜在靶点,为未来的胰腺癌治疗策略提供了新的视角。
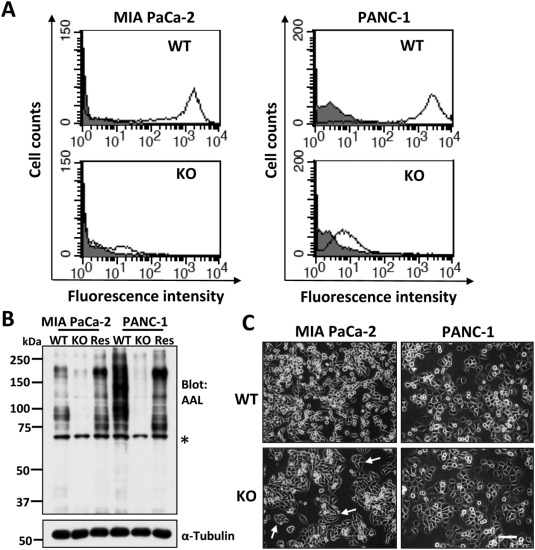
图1 FUT8-KO细胞的建立
二、ATM基因敲除细胞诱导FANCD2蛋白酶体降解
原文链接:https://doi.org/10.1186/s12885-023-10772-y
神经母细胞瘤(Neuroblastoma, NB)是一种常见的儿童实体瘤,临床表现和预后具有高度的异质性,尽管采用了多种治疗策略,但高风险NB患者的肿瘤对标准治疗存在抵抗性,并可能发展成转移。ATM基因与DNA损伤反应有关,位于11q的ATM基因的杂合性缺失和ATM基因的半合性突变在NB肿瘤中是互斥的。在NB细胞系中,ATM的敲低已被证明可以在体外和体内促进肿瘤形成,但ATM与肿瘤形成和癌症侵袭性之间的关联尚不清楚。
研究人员使用CRISPR/Cas9技术敲除了NGP和CHP-134 NB细胞系中的ATM基因,分析ATM基因敲除细胞的增殖和集落形成能力,Western blot检测与DNA修复途径相关的不同蛋白的表达,并在ATM基因敲除细胞中稳定转染FANCD2表达质粒以过表达FANCD2,免疫荧光显微确定蛋白表达情况。结果显示,ATM的缺失导致FANCD2蛋白水平下降,完全ATM基因敲除细胞对PARP抑制剂奥拉帕尼表现出更高的敏感性,在ATM基因敲除细胞中重新引入FANCD2表达,可以恢复细胞的增殖能力。ATM基因敲除细胞揭示了ATM基因杂合性在神经母细胞瘤中的作用机制,并阐明了ATM失活如何增强NB细胞对奥拉帕尼治疗的敏感性,对治疗显示ATM基因剂量和侵袭性癌症进展的高风险NB患者具有重要意义。
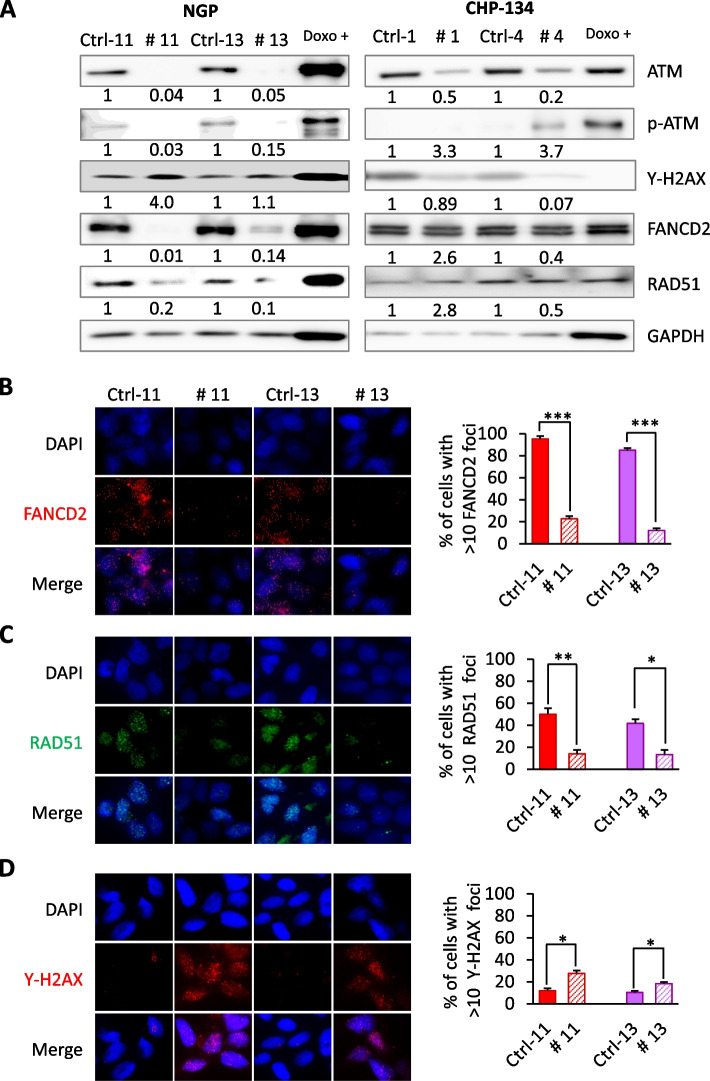
图2 ATM基因缺失损害FANCD2的表达
三、BRCA1基因调控Swan71滋养细胞HMGA2水平
原文链接:https://doi.org/10.1002/mrd.23255
在早期胎盘发育中,肿瘤抑制基因和癌基因共同工作,以一种受控的方式调节细胞增殖和分化。BRCA1是一个已知的肿瘤抑制基因,它与ZNF350和CtIP形成复合体,结合到HMGA2基因的启动子区域,阻止其转录。这种调控在癌症细胞中已有研究,但在胎盘细胞中的研究较少。
研究人员使用CRISPR-Cas9系统在Swan71细胞系中敲除BRCA1基因,生成了BRCA1基因敲除(BRCA1 KO)细胞,通过感染Swan71细胞与含有miR-182过表达构建的慢病毒颗粒,使miR-182在细胞中过表达。结果显示,与野生型细胞相比,BRCA1 KO细胞显示出显著增加的HMGA2 mRNA和蛋白水平;miR-182的过表达导致BRCA1蛋白水平下降,HMGA2蛋白水平上升。BRCA1基因敲除细胞表明BRCA1在调节滋养层细胞中的HMGA2水平方面发挥重要作用,并且可能通过影响细胞凋亡参与胎盘的发育和功能,为理解BRCA1在胎盘发育中的作用提供了新的视角。
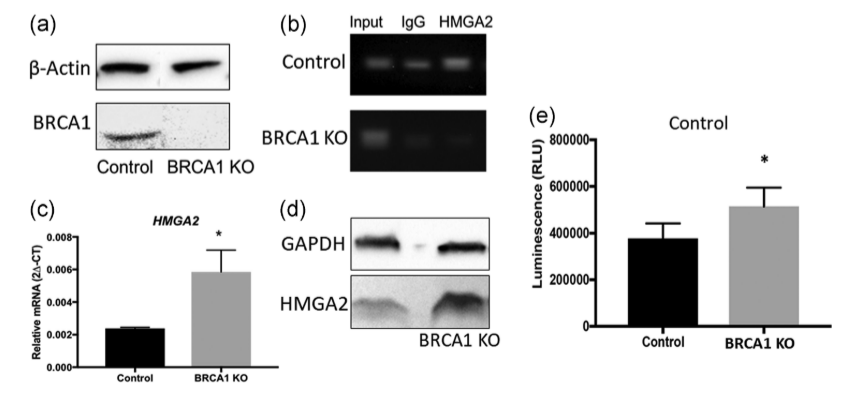
图3 HMGA2在Swan71 BRCA1 KO细胞中的表达
艾迪基因拥有3800+基因敲除细胞现货,覆盖上述文章中的fut8、atm和brca1等热门靶点细胞,为您提供一站式科研支持。现在下单,一周送达,4980元起!
近期资讯
1.【前沿资讯】Prime Editing新动向-提高Prime Editing编辑效率的三种方式
2.【文献解读】利用Cas12a敲除技术探索跨物种lncRNA功能保守性
联系我们
18102225074(微信同号)
market@edgene.cn



