【本月之星】人全基因组 CRISPR/Cas9-KO文库和人RNA结合蛋白文库

CRISPR文库筛选是一种基于CRISPR/Cas9技术的高通量基因筛选方案,通过构建包含成千上万个sgRNA的文库,并将这些sgRNA克隆到慢病毒载体中,以低MOI感染靶细胞。这种方法可以确保每个细胞只被一种sgRNA感染,从而实现针对不同sgRNA对应基因的功能筛选。对此,小编为大家推荐艾迪基因畅销的三款文库现货,并附上该文库相关研究文献解读,希望能为大家的科研道路添砖加瓦。
一、MEC全基因组CRISPR-Cas9敲除筛选助力鉴定调节细胞表面四次跨膜蛋白表达的基因
原文链接:https://doi.org/10.1016/j.celrep.2023.112065
四次跨膜蛋白是一个膜蛋白超家族,它们是在寻找哺乳动物癌细胞的新细胞表面抗原时首次被发现的,目前在人类中一共发现了33个四次跨膜蛋白超家族成员,它们被依次命名为TSPAN1~TSPAN33。四次跨膜蛋白介导多种生物过程,包括免疫反应和肿瘤的发育,但目前关于控制它们在细胞表面表达的机制仍不清楚。因此为了确定四次跨膜蛋白转运的调节因子,研究人员对TSPAN8展开了研究。
MEC是一种来源于胆管癌患者的肝癌细胞系,在所有肝癌细胞系中,MEC细胞在mRNA和蛋白水平上表达的TSPAN8水平最高。为了找到影响TSPAN8表达的基因,研究人员对MEC进行全基因组CRISPR-Cas9敲除筛选。筛选结果显示SPPL3、MGAT1和MGAT2为最具潜力的影响TSPAN8表达的基因。为了验证该基因是否会影响TSPAN8的表达,研究人员使用CRISPR-Cas9基因敲除MGAT1和MGAT2实验和挽救实验的方法进行验证,结果显示MGAT1和MGAT2的敲除明显降低了TSPAN8的表达,且在MGAT1-KO的MEC细胞中重新表达MGAT1能够完全恢复细胞表面TSPAN8的表达。以上结果表明MGAT1、MGAT2基因对TSPAN8的表达有明显的影响。
作者使用MEC全基因组CRISPR-Cas9敲除文库筛选的方法筛选出影响四次跨膜蛋白TSPAN8表达的关键基因,并发现影响其表达的关键途径,为肿瘤侵袭的机制提供了重要参考。
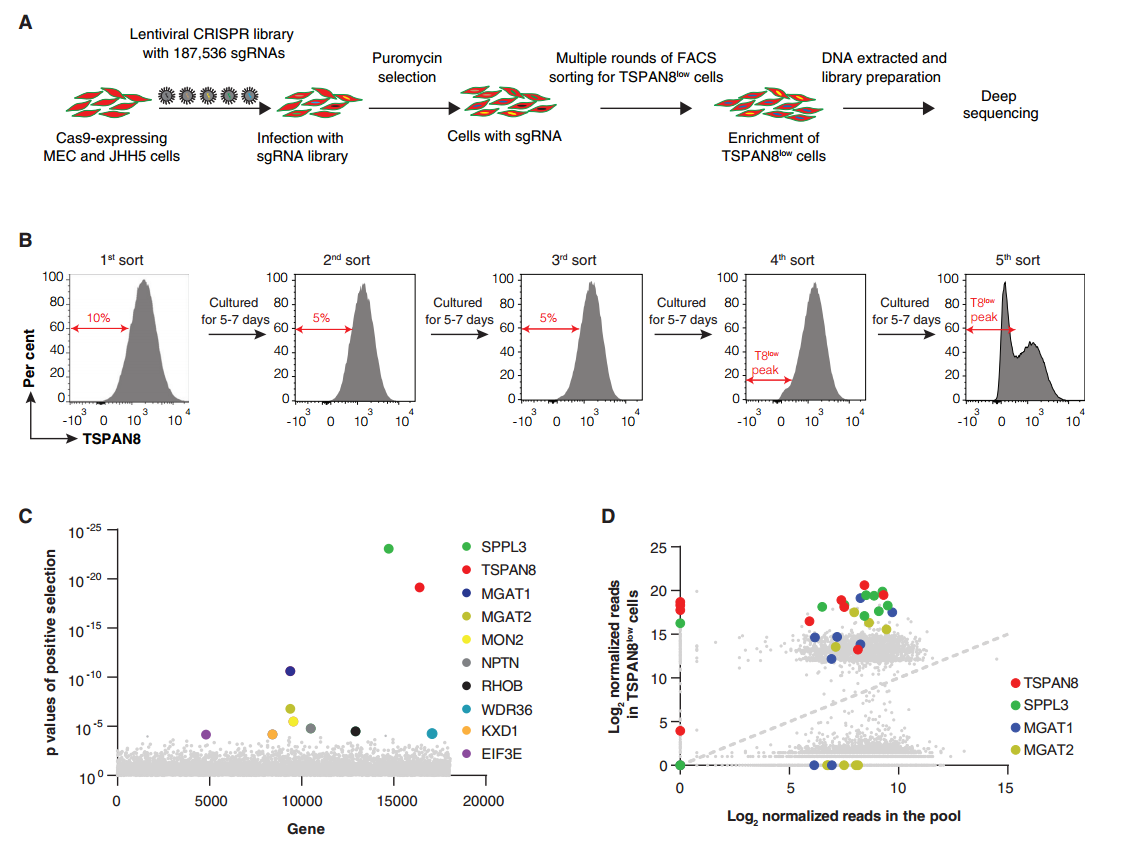
图1 MEC全基因组CRISPR-Cas9敲除筛选,鉴定调控TSPAN8细胞表面表达的基因
二、CRISPR文库筛选技术协助确定了HRP2是多发性骨髓瘤治疗敏感的关键基因
原文链接: https://doi.org/10.1172/JCI149526
多发性骨髓瘤(MM)是一种遗传复杂且异质性的血液系统恶性肿瘤,其特征是恶性浆细胞的单克隆扩增和许多遗传异常,包括染色体易位、缺失、重复和基因突变。HRP2也称为HDGFRP2,是肝瘤衍生生长因子相关蛋白家族的结构相关成员。在癌症细胞中,HRP2主要通过与RNA加工调节分子IWS1相互作用来促进肝细胞癌的细胞生长,然而,HRP2在血液系统恶性肿瘤尤其是在多发性骨髓瘤中的表达、生物学功能和调节机制尚不清楚。
研究人员使用靶向所有人类基因的70290个sgRNA文库进行了全基因组CRISPR/Cas9-KO筛选。通过负选择筛选硼替佐米的耐药基因,通过正选择筛选对硼替佐米敏感的基因。在基因组中扩增sgRNA序列后,通过高通量测序计算细胞中sgRNAs的覆盖率,在敏感细胞中通过正选择发现了28个基因,在抗性细胞中通过负选择发现了15个基因,随后验证了先前建立的对硼替佐米耐药MM细胞中正负选择的前10个基因的表达,确定HRP2是富集基因中差异表达最多的基因。在硼替佐米抗性细胞中,所有靶向 HRP2 的sgRNAs显著增加,RRA算法也证实 HRP2 是最重要的基因之一。之后,为了验证HRP2与 MM 细胞中H3K27me3水平高低的关系,研究人员敲低 HRP2 ,并观察这些必需基因的表达是否增多或减少。结果显示参与 ER 应激相关凋亡途径的一些重要基因上的 H3K27me3 表达升高,说明这些重要基因受到 HRP2 和 H3K27me3的严格调控。这些数据表明,HRP2与临床上MM患者的治疗反应和结果密切相关。
该研究通过人类全基因组CRISPR文库筛选技术,筛选确定HRP2基因是MM对硼替佐米治疗敏感的关键基因,有助于多发性骨髓瘤治疗机制方面的研究,为治疗策略提供新的思路。
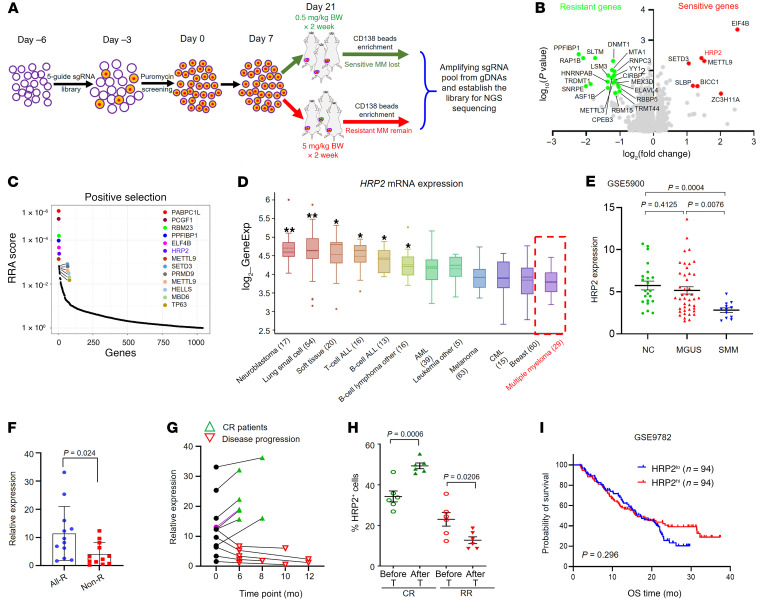
图2 体内 CRISPR 文库筛选发现 HRP2 是硼替佐米耐药的关键负调节因子
三、RNA结合蛋白文库助力INTS3基因在大肠癌中的作用研究
原文链接:https://doi.org/10.1016/j.isci.2024.109676
大肠癌(Colorectal Cancer, CRC)是一种源于结肠或直肠上皮细胞的恶性肿瘤,具有高发病率和死亡率。研究表明某些RNA结合蛋白(RBPs)对大肠癌(CRC)细胞存活至关重要,其主要作用机制包括:抗凋亡功能、促进肿瘤生长、RNA代谢调控等。为了寻找与CRC相关的基因,研究人员进行了系列研究。
研究人员使用包含了1078个RBPs靶点的的sgRNA文库,在大肠癌(CRC)细胞系中进行CRISPR高通量筛选。目的是通过测定sgRNA丰度的变化,鉴定敲除后显著影响细胞存活或增殖的关键RBPs基因。结果显示,通过CRISPR文库筛选,系统性地筛选出了27个与大肠癌(CRC)细胞存活相关的RBPs,其中INTS3基因相关性最高。为了验证INTS3的功能,实验人员设计了针对该基因的sgRNA,经敲除后发现CRC细胞的凋亡率得到了大幅度提高,同时体内外肿瘤的生长得到了显著抑制,这一结果进一步证实了INTS3对癌细胞存活的关键作用。通过CRISPR-Cas9技术敲除INTS3并结合转录组测序,研究人员发现其通过调控抗凋亡基因(如TXNIP、CLU和NR4A1)mRNA的稳定性,增强了CRC细胞的存活能力。
研究结果不仅对RBPs在大肠癌中功能进行了深入的探究,还为癌症的精准治疗提供了新的靶点和策略。CRISPR文库筛选技术凭借其高通量、特异性和高效性的优势特点,成为了解析基因功能网络和识别关键治疗靶点的前沿工具,为精准医学研究提供了重要支撑。

图3 大肠癌(CRC)细胞中RNA结合蛋白(RBPs)的CRISPR-Cas9筛选
艾迪基因专研基因编辑十余载,拥有最全系列高效Cas9稳转株,集齐科研圈最火CRISPR sgRNA文库类型,专家团队贴心服务,下单即筛!
近期资讯
1.【一周时讯】全基因组CRISPR筛选:揭示新宿主因子,优化轮状病毒疫苗生产
2.【文献解读】CRISPR-Cas12a反式切割活性增强新策略:利用变体减少顺式切割产物的空间位阻
3.【一周时讯】CRISPR筛选:揭示TMEM106B可介导SARS-CoV-2的ACE2独立感染途径

联系我们
18102225074(微信同号)
market@edgene.cn


 Login
Login










Comment (4)